
期刊简介
《西南国防医药》杂志是成都军区卫生部主管,成都军区医学科学技术委员会主办的综合性医学学术刊物。创刊于1973年,创刊时刊名为《资料汇编》,为不定期刊物,刊载内容以医学临床专题讲座、综述为主。1979年更名为《医学资料汇编》,定期季刊出版,刊载内容较以前有了很大改变,主要以科研课题论文、临床研究论文为主。1985年原昆明军区与成都军区合并后,改名为《西南部队医药》,仍为季刊。1991年经解放军总政治部和国家新闻出版署审查批准《西南部队医药》更名为《西南国防医药》(双月刊),在国内外公开发行,是全军各大军区、军兵种主办的同类期刊中第一个公开发行的医学刊物。2000年经国家科技部科技信息研究所审查批准,《西南国防医药》被收录为中国科技论文统计源期刊,列为国家科技核心期刊。2009年1月经解放军总政治部和国家新闻出版批准,《西南国防医药》改为单月刊,是全军同类期刊中第一本月刊。目前,《西南国防医药》已被美国化学文摘(CA)、波兰哥白尼索引、英国国际农业与生物科学研究中心及中国科技论文统计源等国内外十余个主要期刊数据库收录,是万方期刊网、清华学术光盘版、中文科技期刊数据库全文上网期刊,是国家级核心刊物,也被多个省(市、区)列为A类期刊,作为晋升高级专业技术职务的认可刊物。《西南国防医药》以传递医学科技信息、加强学术交流、促进医学科学技术发展为宗旨,以各类医务人员为主要读者对象。辟有专家论坛、论著、临床研究、高原医学、中医•中西医结合、护理园地、医院管理、卫勤研究、基层卫生、综述•讲座等栏目,集学术性、技术性及实用性为一体,具有军事医学和高原及亚热带疾病防治等特色。
靶向CD7的“现货型”CAR-T细胞疗法在复发/难治性T细胞恶性肿瘤中的疗效
时间:2023-11-21 09:58:42
T细胞急性淋巴细胞白血病(T-ALL)是一种高度侵袭性的血液系统恶性肿瘤,其占成人ALL病例的25%,占儿童ALL的15%。与B-ALL相似,T-ALL成人患者也存在治愈可能,其5年总生存(OS)率为48%。然而,复发/难治性(R/R)T-ALL成人患者的预后结局较差,其长期生存率低于10%。这些患者需要包括靶向药物和嵌合抗原受体T细胞(CAR-T)疗法在内的新型疗法来改善远期生存。
跨膜蛋白CD7在95%的T-ALL患者中高表达,因此其为T-ALL治疗的理想靶点。GC027是一种靶向CD7的“现货型”同种异体CAR-T产品,研究者先前开展了一项初步临床试验,数据表明GC027在R/R T-ALL患者中产生了快速、深入和持久的缓解。基于此,陆军军医大学第二附属医院(新桥医院)张曦教授、中国人民解放军联勤保障部队第九二O医院王三斌教授团队扩大了研究队列,报告了GC027作为独立治疗方案在R/R T-ALL成人患者的扩大患者组中的最新疗效结果。
研究方法
该试验为多中心I期临床试验(ChiCTR1900025311)。试验的关键纳入标准包括年龄为18-70岁,确诊为R/R T-ALL,入组时流式细胞术或免疫组化检测确定具有CD7+白血病原始细胞。通过骨髓活检,纳入的患者在形态学上确诊为T-ALL,且ECOG体能状态评分为0-2。伴有活动性感染或主要器官功能障碍的患者被排除在外。该临床试验的主要目的是评估GC027的安全性,次要目的是评估其药代动力学特征和疗效。主要终点是4周内的剂量限制毒性(DLT)和3个月内的不良事件(AE);次要终点是GC027输注后3个月内的总缓解率(ORR),外周血和骨髓中CAR-T细胞数和CAR拷贝数。该试验计划患者接受>4×106 CAR+T细胞/kg。鉴于GC027与患者自身CD3+CD7-细胞排斥的特点,研究者设置了两个剂量阶段:低剂量阶段和剂量扩展阶段。低剂量阶段的剂量为6×106 CAR+T细胞/kg,计划入组3例患者,剂量扩展阶段包含两个剂量组:1×107 CAR+T细胞/kg和1.5×107 CAR+T细胞/kg。
研究结果
01患者临床特征
该临床试验最终纳入了12例患者,其中11例为R/R T-ALL,1例为R/R T淋巴母细胞淋巴瘤(T-LBL)。所有患者(n=12)的中位年龄为28(19-47)岁。依据流式细胞术检测,骨髓肿瘤负荷的中位值为24.5%(0-66.28%)。入组时,4例患者伴有髓外疾病,3例在异基因造血干细胞移植(allo-HSCT)后复发。3例患者接受了6.2–8.6×106 CAR+T细胞/kg,9例接受了1–1.5×107细胞/kg。在输注CAR-T细胞前,所有患者均接受了4-6天的清淋预处理方案。清淋预处理方案的化疗药物包括剂量增强的氟达拉滨+环磷酰胺,联合美法仑/依托泊苷/泼尼松。具体临床特征见表1。
表1.所有患者的临床基线特征及疗效结果
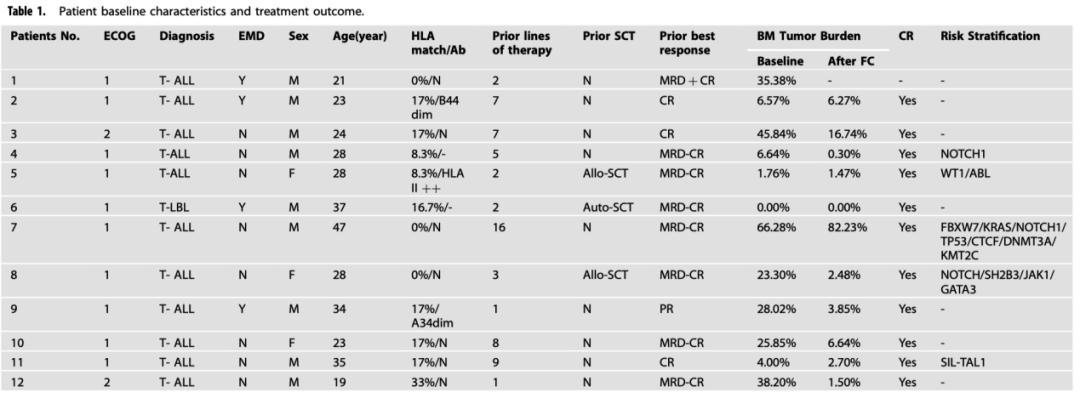
02疗效及安全性结果
在所有患者(n=12)中,11例患者在CAR-T细胞输注后1个月内达到完全缓解(CR)或伴血液学不完全恢复的CR,CR率为91.7%;在所有患者中,CAR-T细胞从输注后迅速扩增,并在输注后5-10天达到峰值。在4例伴有髓外疾病的患者中,3例达到CR。在达到CR的患者(n=11)中,1例接受了allo-HSCT,其余10例在缓解后均未接受其他抗白血病治疗。8号患者(P08)在GC027输注后达到CR,接受allo-HSCT以降低复发风险,移植后1个月因严重GVHD死亡;P10因严重感染死亡。4例患者在5-10个月内复发。数据截止于2022年11月30日,2例患者仍处于缓解期,P03缓解时间大于3年。
该试验中,研究者未观察到免疫效应细胞相关神经毒性综合征(ICANS)的发生。10例(83%)患者出现了任何级别的细胞因子释放综合征(CRS),其中2例为2级,8例为3级。CRS发生于CAR-T细胞输注当天或第二天。及时治疗后,8例3级CRS患者均缓解。Fisher精确检验结果表明,CAR-T输注剂量与CRS等级之间没有显著的相关性(相关性=0,p=1.00)。疗效和安全性结果见图1。
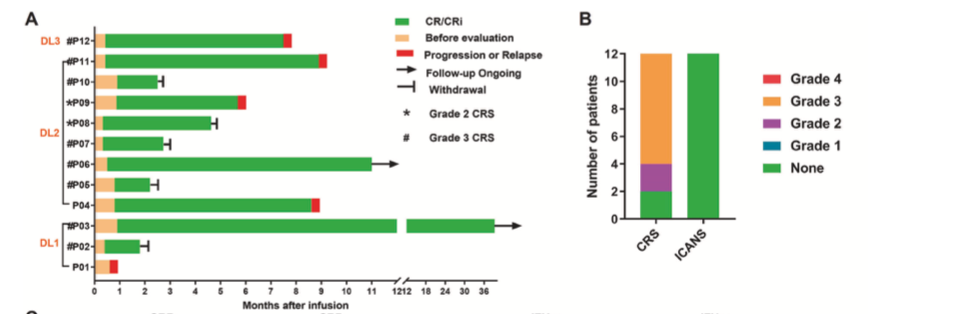
图1.所有患者CAR-T输注后的生存情况(A);CRS和ICANS的结果(B)
研究结论
该研究表明,同种异体“现货型”CAR-T细胞疗法GC027作为一种独立疗法,在接受重度预处理的T细胞恶性肿瘤患者中显示出良好的早期疗效。单次输注GC027能够在输注后4周内诱导深度和持久的缓解,且临床毒性可控。为取得更好的临床疗效,应考虑加强对感染患者的护理,并桥接allo-HSCT。
